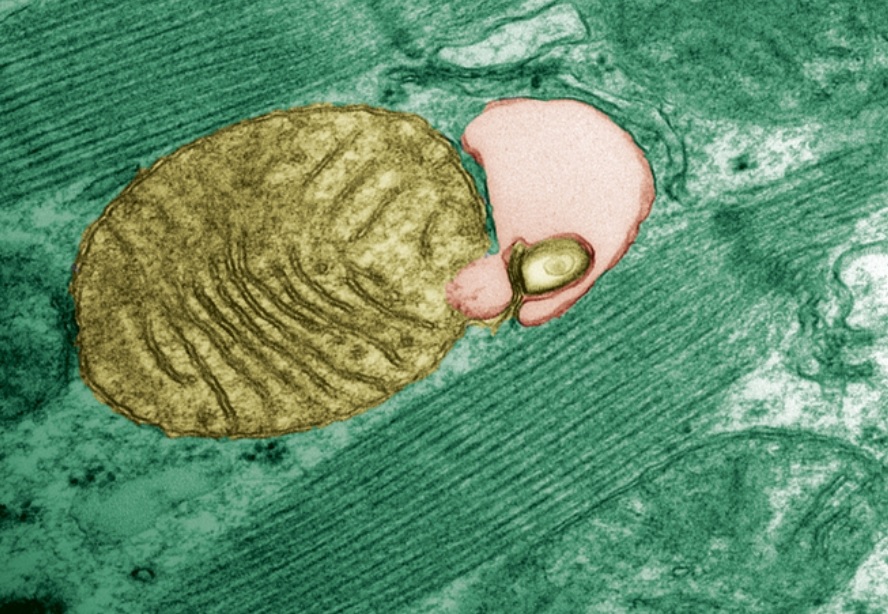
Une nouvelle cible thérapeutique possible pour le traitement des maladies associées aux mutations de l’ADN mitochondrial, c’est la découverte de cette équipe de la São Paulo Research Foundation (FAPESP), qui décrypte, dans la revue Autophagy, le processus par lequel les mitochondries défectueuses sont englouties par « l’autophagosome » (Visuel).
Avec le vieillissement, le matériel génétique mutant a tendance à s’accumuler dans les mitochondries, des organites responsables de la production d’énergie nécessaire aux cellules, ce qui peut entraîner des maladies. Les chercheurs brésiliens démontrent que le mécanisme de nettoyage cellulaire appelé autophagie peut moduler ce phénomène d’accumulation délétère.
L’autophagie, le mécanisme biologique probable qui module l’accumulation d’ADN mitochondrial mutant
Cette accumulation d’ADN mitochondrial mutant se produit dans les cellules au cours du vieillissement, en particulier dans le foie. Mais le mécanisme d’autophagie, un processus de nettoyage cellulaire qui détruit les organites, y compris les mitochondries « usées », et recycle leurs composants pourrait jouer un rôle clé dans l’émergence de maladies associées à l’ADN mitochondrial, ouvrant la voie au développement de thérapies.
Les mitochondries sont responsables de la respiration cellulaire, traitant des substrats pour fournir de l’énergie à l’organisme. Les mitochondries ont leur propre génome, hérité uniquement de la mère, contrairement à l’ADN trouvé dans les noyaux cellulaires, qui est hérité des deux parents.
Les maladies mitochondriales : l’ADN mitochondrial est également sujet à des mutations, dont certaines peuvent entraîner des maladies « mitochondriales ». Selon les estimations, les troubles causés par les mutations de l’ADN mitochondrial affectent au moins une personne sur 5.000 dans le monde.
- L’un de ces troubles est le syndrome de MELAS (encéphalopathie mitochondriale, acidose lactique et épisodes de type AVC), qui peut provoquer des convulsions, des douleurs, une altération de la conscience et des déficits neurologiques focaux, entre autres symptômes.
Outre les troubles directement liés aux mutations de l’ADN mitochondrial, il existe d’autres maladies auxquelles ces mutations contribuent au moins en partie, explique l’un des auteurs principaux, Marcos Chiaratti, professeur au Département de génétique et d’évolution de l’Université fédérale de São Carlos (UFSCar) : c’est notamment le cas du diabète, de la maladie de Parkinson et de la maladie d’Alzheimer. En conséquence, pouvoir traiter les mutations de l’ADN mitochonrial pourrait également contribuer à traiter ces maladies.
Les mutations de l’ADN mitochondrial s’accumulent au cours du vieillissement. Prenant en compte l’importance de l’autophagie dans le cycle de vie des cellules et du recyclage mitochondrial, les chercheurs ont regardé si ce processus pouvait jouer un rôle dans le développement de ces mutations de l’ADN mitochondrial et si, avec l’âge, il pouvait fonctionner de manière de moins en moins efficace.
L’étude est menée chez la souris, avec hétéroplasmie à 30 % soit avec 30% de l’ADN du génome mitochondrial mutant, croisée avec d’autres privées du gène permettant le processus d’autophagie. Les chercheurs ont ainsi obtenu 2 types de souris, un groupe témoin avec de l’ADN mitochondrial mutant et le gène permettant l’autophagie et un groupe avec l’ADN mutant mais sans le gène permettant l’autophagie dans le foie. Les expériences montrent que :
- l’autophagie affecte l’accumulation d’ADN mitochondrial mutant au fil du temps.
- Dès 21 jours, cet ADN mitochondrial commence à s’accumuler dans le foie des animaux privés de cette capacité d’autophagie. De plus, l’autophagie élimine principalement l’ADN mitochondrial défectueux.
« Nous avons donc postulé que l’autophagie pourrait aider à éliminer les mitochondries les moins fonctionnelles tout en conservant les plus aptes, ce qui constitue un effet positif, bien sûr ».
- Une autre expérience in vitro, menée sur des lignées de fibroblastes, un type de cellule du tissu conjonctif de souris, confirme que lorsque l’autophagie est bloquée, l’élimination de l’ADN mutant l’est également.
L’étude révèle ainsi le rôle clé du processus d’autophagie dans l’élimination de l’ADN mitochondrial défectueux, une accumulation naturelle avec le vieillissement. Mais elle se poursuit maintenant avec les différents ADN mitochondriaux connus pour être pathologiques : l’objectif est bien d’identifier des traitements qui stimulent le mécanisme de nettoyage cellulaire contre les maladies caractérisées par un dysfonctionnement des mitochondries.
Source: Autophagy Feb 2022 DOI: 10.1080/15548627.2022.2038501 Autophagy deficiency abolishes liver mitochondrial DNA segregation
Plus sur les Maladies mitochondriales

Laisser un commentaire