Certes ce candidat est beaucoup moins avancé, mais il promet des avantages incomparables au-delà d’une immunisation efficace : un schéma à injection unique, l’absence de contrainte de chaîne du froid pour le stockage, le transport et la distribution et un tarif bon marché. Développé par une équipe de virologues de l’Université de Stanford et présenté dans la revue ACS Central Science, le candidat basé sur des nanoparticules de ferritine recouvertes de fragments de la protéine de pointe du coronavirus, vient de faire ses premières preuves chez la souris.
Le laboratoire du biochimiste Peter S. Kim de l'Université de Stanford est spécialisé dans le développement de vaccins contre le VIH, Ebola et la grippe. Dès l’émergence de COVID-19, l’équipe s’est mise au développement d’un vaccin contre le SRAS-CoV-2 et présente aujourd’hui un candidat prometteur. « L’objectif derrière ce challenge est de pouvoir donner accès au vaccin aux pays à revenu faible ou intermédiaire », explique Kim, également professeur de biochimie à Stanford.
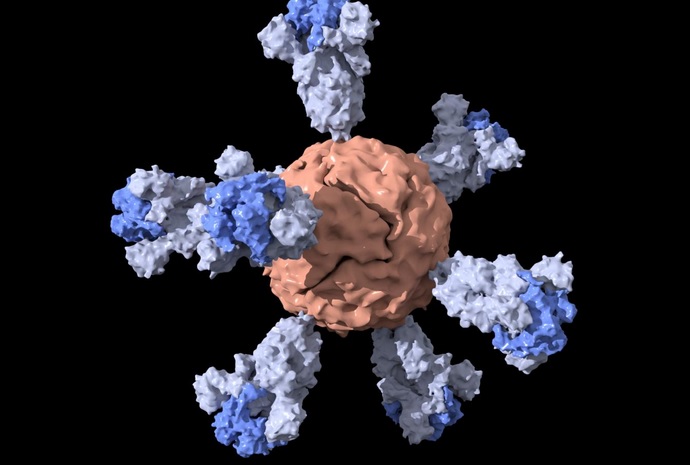
Déclencher toujours la réponse immunitaire par des fragments de protéine S
Le candidat est basé sur des nanoparticules parsemées de fragments des protéines de pointe du virus. Les chercheurs rappellent que ces points ou pics facilitent l'infection en se liant à une cellule hôte et en créant un passage pour que le génome viral pénètre et détourne la machinerie de la cellule pour produire plus de virus. Les pointes peuvent également être utilisées comme antigènes, c’est-à-dire pour déclencher dans le corps une réponse immunitaire. Ici, les scientifiques ont choisi de supprimer une section près de la base ou « du bas » de la protéine de pointe, puis pour former leur vaccin, ont combiné ce pic raccourci avec des nanoparticules de ferritine, une protéine contenant du fer, déjà testée chez l'Homme (pour un vaccin contre Ebola notamment).
La particularité du candidat réside donc plutôt dans ses nanoparticules qui le stabilisent, le rendent plus « sécuritaire » et apportent une plus grande facilité de production. Les vaccins qui utilisent des virus pour délivrer l'antigène sont souvent plus efficaces que les vaccins qui ne contiennent que des parties isolées d'un virus. Cependant, ils peuvent prendre plus de temps à produire, doivent être réfrigérés et sont plus susceptibles de provoquer des effets secondaires. Les vaccins à base d’ARNm comme ceux de Pfizer et Moderna qui ont récemment été autorisés pour une utilisation d'urgence par la FDA sont encore plus rapides à produire que les vaccins à nanoparticules -comme ce candidat de Stanford-, mais ils sont très chers à fabriquer et nécessitent plusieurs doses.
Une seule dose pourrait suffire : c’est ce que montrent les premiers tests menés chez la souris qui suggèrent une immunité au COVID-19 après une seule dose. Les chercheurs espèrent également qu'il pourra être conservé à température ambiante et sont même en train de « regarder » comment il pourrait être expédié et stocké sous forme de poudre lyophilisée. Ce serait un avantage considérable vs les vaccins actuellement autorisés qui doivent tous être conservés à des températures froides, jusqu’à -70 degrés C, pour le vaccin de Pfizer.
De premiers tests positifs chez l’animal : les chercheurs ont comparé, chez la souris, plusieurs candidats, à base de ces nanoparticules à pointes raccourcies ainsi que 4 autres variantes, dont une avec des pointes complètes, des pointes complètes sans nanoparticules, ainsi qu’un candidat contenant uniquement la section du pic qui se lie aux cellules pendant l'infection. Ensuite, les chercheurs ont utilisé un pseudo-coronavirus plus sûr, modifié pour porter les pics du SRAS-CoV-2, pour infecter les souris. Ainsi, les scientifiques ont pu déterminer l'efficacité de chaque variante en mesurant les niveaux d'anticorps neutralisants.
- Après une dose unique, les deux candidats vaccins nanoparticulaires ont tous deux abouti à des niveaux d'anticorps neutralisants 2 fois plus élevés que les niveaux équivalents observés chez les personnes ayant développé COVID-19, et le vaccin à nanoparticules à pointe raccourcie a produit une réponse neutralisante encore plus élevée.
4 semaines ont suffi à en arriver là ! S’il reste encore un long chemin à parcourir avant l’approbation, commente l’auteur principal, Abigail Powell, chercheur au laboratoire de Kim, « nous pensons que nous avons là un point de départ solide pour un schéma de vaccination à dose unique, facile à produire et à transporter ». Les chercheurs soulignent une prouesse, soit un délai entre le début des recherches et les premières études sur la souris de seulement 4 semaines.
«Tout le monde avait beaucoup d'énergie à consacrer à cette priorité scientifique. C'est un scénario tout à fait unique que je ne m'attends pas vraiment à revivre un jour dans ma carrière ».
Si la prochaine étape reste la tenue d’essais cliniques, l’équipe travaille déjà également au développement d’un vaccin universel contre les coronavirus (SRAS-CoV-1, MERS, SRAS-CoV-2 et les autres coronavirus qui pourraient émerger).
Source: ACS Central Science January 5, 2021 DOI : 10.1021/acscentsci.0c01405 A Single Immunization with Spike-Functionalized Ferritin Vaccines Elicits Neutralizing Antibody Responses against SARS-CoV-2 in Mice
Lire aussi :

Laisser un commentaire