Des scientifiques de l’University of British Columbia (Vancouver) réalisent ici une première : l’impression en 3D de cellules testiculaires (à terme productrices de spermatozoïdes), avec un objectif à plus long terme de production de sperme. Un objectif pas si irréaliste alors que leurs travaux, présentés dans la revue Fertility and Sterility® Science (F&S Science) montrent que, 12 jours après l’impression 3D, ces cellules sont non seulement toujours vivantes mais se sont même différenciées en cellules spécialisées impliquées dans la production de sperme.
Ce sont les signes précoces et prometteurs d’une capacité future de production de sperme, alors que la prévalence de l’infertilité augmente en particulier sous l’effet de facteurs de mode de vie mais aussi d’âge à la conception. L’équipe, menée par le Dr Ryan Flannigan de l’University of British Columbia espère donc véritablement pouvoir apporter « un jour une solution aux personnes vivant avec des formes d’infertilité masculine actuellement incurables ».
L’infertilité touche 15 % des couples
et les facteurs masculins en sont la cause dans au moins 50 % cas.
Peu d’options en cas d’azoospermie : Le concept est donc d’imprimer en 3D ces cellules sous une forme qui imite l’anatomie humaine : dans les testicules humains, le sperme est produit par de minuscules tubules séminifères. Dans la forme la plus grave d’infertilité masculine, l’azoospermie non obstructive plus aucun spermatozoïde n’est trouvé dans dans les tubes séminifères. Dans certains cas, une intervention chirurgicale visant à retrouver des spermatozoïdes, par ailleurs extrêmement rares, est envisagée, mais cette procédure n’aboutit qu’une fois sur 2.
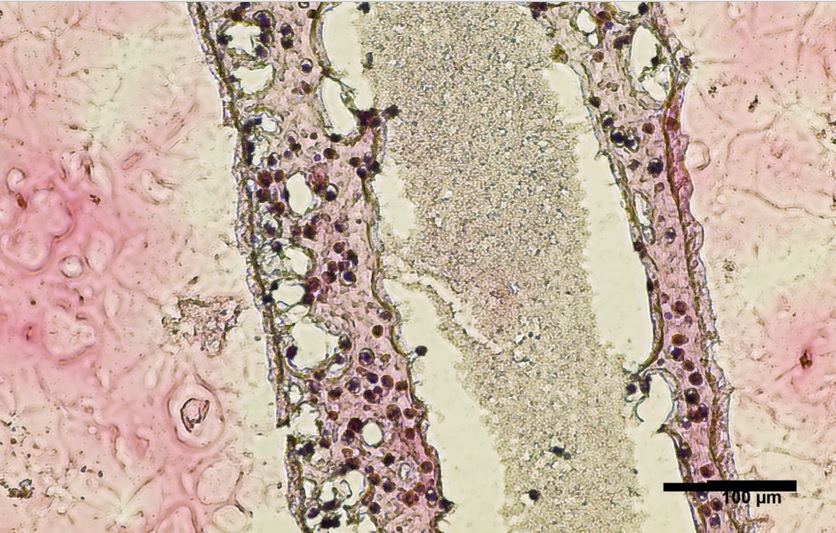
Imprimer et spécialiser des cellules de remplacement : ici, les chercheurs ont effectué une biopsie pour collecter des cellules souches des testicules d’un patient atteint d’azoospermie non obstructive. Les cellules ont été cultivées et imprimées en 3D dans ne boîte de Pétri dans une structure tubulaire creuse qui ressemble aux tubes séminifères humains producteurs de sperme (visuel). L’expérience montre que :
- 12 jours après impression, les cellules ont survécu ;
- ces cellules se sont différenciées en plusieurs des cellules spécialisées impliquées dans la production de sperme ;
- une amélioration significative de l’activité des cellules souches spermatogoniales est observée (ce sont les cellules souches germinales support de la production des spermatozoïdes) ce qui constitue un signe encourageant sur la capacité de production de sperme.
« Observer ces cellules survivre et commencer à se différencier est un signe encourageant. Il y a un long chemin à parcourir, mais cela apporte un grand espoir contre ces formes d’infertilité ».
L’équipe travaille maintenant à « entraîner » les cellules imprimées à produire du sperme. Pour ce faire, ils vont exposer les cellules à différents nutriments et facteurs de croissance et optimiser leurs conditions de production. Si ces cellules se confirment capables de produire du sperme, ces spermatozoïdes pourraient être théoriquement utilisés pour féconder un ovule par fécondation in vitro, offrant ainsi une nouvelle option de traitement de la fertilité aux couples infertiles.
Un nouvel éclairage sur les mécanismes génétiques et moléculaires en cause dans l’azoospermie, est également apporté : différentes techniques de séquençage permettent comprendre l’expression génique et les caractéristiques de chaque cellule individuelle, puis la modélisation informatique de ces données permet alors de mieux cerner les causes profondes de la condition, voire d’identifier de nouvelles options de traitement.
« Nous découvrons de nouvelles causes d’infertilité, chaque cas est très spécifique à chaque patient. En la matière, nous devons donc adopter une approche de médecine de précision:
- prélever des cellules d’un patient,
- identifier leurs anomalies,
- imprimer des cellules souches en 3D
- et induire ces cellules à se différencier de manière à surmonter leurs déficiences initiales ».
Source: Fertility and Sterility® Science (F&S Science) 16 Feb, 2022 DOI: 10.1016/j.xfss.2022.02.004 Using Clinically Derived Human Tissue to 3D Bioprint Personalized Testicular Tubules For in-Vitro Culturing
Plus sur l’Infertilité


Laisser un commentaire