
Cette équipe de l’Université Duke (Caroline du Nord) révèle qu’un repas riche en graisses coupe, quelques heures, la communication entre l'intestin et le reste du corps. A l’origine de ce mécanisme probablement protecteur, une famille de bactéries spécifique du microbiote. Un silence « intestinal » qui n'est pas anodin : la compréhension de ce processus, documenté dans la revue eLife, pourrait permettre le développement de nouveaux traitements contre la résistance à l’insuline et le diabète de type 2.
Les chercheurs ont utilisé le poisson zèbre pour examiner les cellules qui signalent normalement au cerveau et au reste du corps ce qui se passe à l'intérieur de l'intestin après un repas. Ces cellules entéro-endocrines (en vert sur visuel), présentes dans la muqueuse de l'intestin (en rouge), libèrent des hormones qui envoient des signaux au système nerveux et au cerveau. Ces cellules produisent ainsi au moins 15 hormones associées aux différents signaux sur les mouvements intestinaux, les sensations de faim et de satiété, la digestion, l'absorption des nutriments, la sensibilité à l'insuline et le stockage de l’énergie.
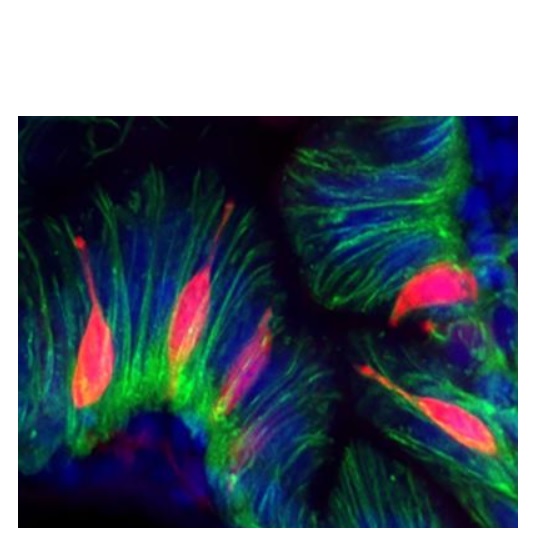
Ces cellules intestinales s'endorment durant quelques heures après un repas riche en graisses
« Nous ne savons pas encore si c'est bon ou mauvais », commente l’auteur principal, John Rawls, professeur agrégé de génétique moléculaire et de microbiologie à la Duke.
Mieux comprendre le cycle postprandial (qui suit le repas) est donc important, car étant donné leur rôle clé dans la digestion et la sensation de satiété, le silence de ces cellules endocrines pourrait induire les personnes qui ont une alimentation déjà riche en graisses à manger encore plus. Et si ce silence se produit chaque fois que nous mangeons un repas malsain et riche en graisses, cela pourrait entraîner un changement de la signalisation de l'insuline, ce qui pourrait contribuer au développement de la résistance à l'insuline et du diabète de type 2. Pour mieux comprendre cet épisode de silence postpandrial, les chercheurs ont décomposé ce processus chez le poisson zèbre.
Le processus vu du poisson-zèbre :
- Dès détection du repas, les cellules entéro-endocrines déclenchent une explosion de calcium en quelques secondes, initiant le processus de signalisation ;
- après ce signal initial, intervient ce silence : durant ce silence, les cellules changent de forme et subissent un stress dans leur réticulum endoplasmique, une structure qui effectue la synthèse des nouvelles protéines ;
- ensuite ces cellules entéro-endocrines, spécialisées dans la synthèse des protéines sont sur-stimulées puis… épuisées pendant un certain temps.
- cependant des poissons zèbres exempts de microbiotes ne présentent pas ce même effet de silence après un repas riche en graisse.
Des microbes intestinaux impliqués dans le processus : après avoir passé en revue toutes les sortes de bactéries présentes dans l'intestin, les chercheurs attribuent ce silence à un seul type de bactéries intestinales, appelé Acinetobacter. Ces bactéries, qui représentent normalement moins de 0,1% du microbiome intestinal total, s’avèrent multipliées par 100 après un repas riche en graisses et ce sont les seules bactéries capables d'induire cet effet de silence.
Pourquoi Acinetobacter fait le silence dans l’intestin ? Les chercheurs suggèrent que cela pourrait être un moyen d'empêcher une signalisation excessive de la graisse. « Nous ne comprenons pas encore quel est précisément l'impact à long terme de l'inhibition entéro-endocrinienne sur la santé métabolique. Est-ce une réponse à une alimentation trop riche ? Il est en effet possible que le silence recouvre un mécanisme d’adaptation bénéfique pour protéger l’organisme d’une stimulation excessive des cellules intestinales ».
Source: eLife Dec 3, 2019 High fat diet induces microbiota-dependent silencing of enteroendocrine cells (Visuel 2 Duke University / Lihua Ye)

Laisser un commentaire